膠質(zhì)母細(xì)胞瘤(GBM)是原發(fā)性腦腫瘤中最具侵襲性的亞型。血腦屏障(BBB)以及治療方法的低腫瘤特異性等問(wèn)題導(dǎo)致GBM對(duì)標(biāo)準(zhǔn)化療難以產(chǎn)生有效的反應(yīng)。有鑒于此,華東師范大學(xué)徐志愛(ài)教授通過(guò)將酸-光雙活化蛋白水解靶向嵌合體(PROTAC)納米粒子和自供氧BSA-MnO2(BM)納米粒子進(jìn)行集成,合理設(shè)計(jì)了一種能夠用于治療GBM的雙層微針(MN)貼片。
本文要點(diǎn):
(1)MN可在腫瘤部位局部遞送PROTAC前藥和BM納米顆粒。研究發(fā)現(xiàn),PROTAC納米顆粒能夠從MN的外層被迅速釋放,并在腫瘤細(xì)胞的胞內(nèi)酸性環(huán)境中被特異性激活。隨后,近紅外光可通過(guò)光動(dòng)力療法(PDT)激活光敏劑產(chǎn)生單線(xiàn)態(tài)氧(1O2),以觸發(fā)溴結(jié)構(gòu)域和外膜蛋白4(BRD4)的時(shí)空可調(diào)降解。
(2)BM納米顆粒位于MN的內(nèi)層,其可作為將過(guò)氧化氫(H2O2)轉(zhuǎn)化為氧氣(O2)的供氧站,以逆轉(zhuǎn)腫瘤乏氧,增強(qiáng)PDT和促進(jìn)PROTAC的活化。實(shí)驗(yàn)結(jié)果表明,集成PROTAC前藥的MN可在皮下和原位GBM腫瘤模型中顯著抑制腫瘤生長(zhǎng)。綜上所述,該研究創(chuàng)新設(shè)計(jì)了一種能夠高效治療GBM的時(shí)空可調(diào)蛋白降解策略,其有望被拓展用于實(shí)現(xiàn)對(duì)其他類(lèi)型難治性腦腫瘤的精準(zhǔn)治療。
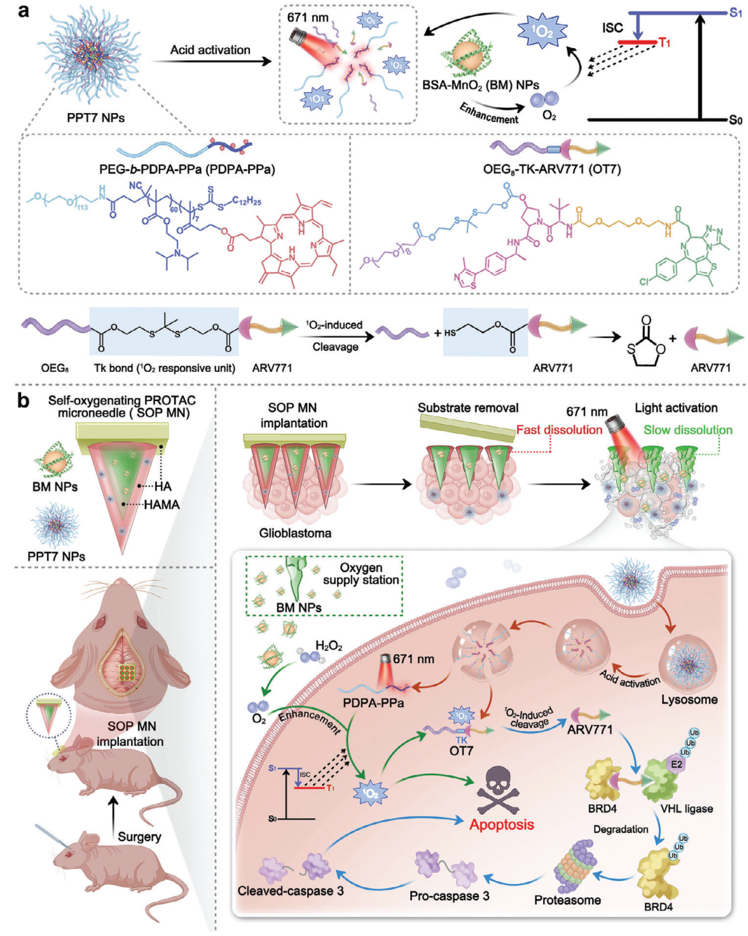
Xingyu Jiang. et al. Self-Oxygenating PROTAC Microneedle for Spatiotemporally-Confined Protein Degradation and Enhanced Glioblastoma Therapy. Advanced Materials. 2025
DOI: 10.1002/adma.202411869
https://advanced.onlinelibrary.wiley.com/doi/10.1002/adma.202411869



















