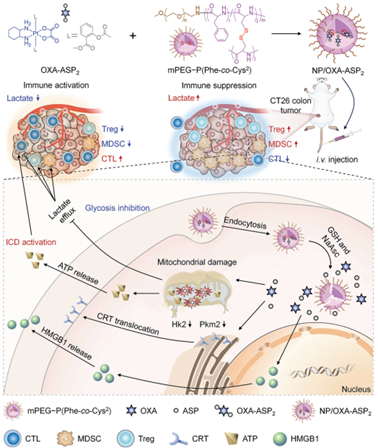
腫瘤細胞的糖代謝異常與免疫抑制性腫瘤微環境(TME)有關。雖然抑制糖酵解可增強T細胞介導的免疫應答,但如何將糖酵解抑制與免疫治療相結合仍是一項亟待解決的難題。有鑒于此,中國科學院長春應化所陳學思院士和丁建勛研究員開發了一種靶向葡萄糖代謝的奧沙利鉑(IV)-阿司匹林前藥聚(氨基酸)納米制劑(NP/OXA-ASP2),其可通過抑制腫瘤糖酵解改善化學-免疫治療。
本文要點:
(1)該聚(氨基酸)納米粒子可實現選擇性釋放,其在還原條件下36 h內能夠釋放90.0%的OXA-ASP2。超過80%的前藥可在12 h內轉化為OXA和ASP,以促進線粒體損傷和糖酵解抑制,放大OXA誘導的免疫原性細胞死亡。研究發現,抑制糖酵解通量可減少乳酸泄漏,緩解免疫抑制性TME。這些協同機制有助于增強化學-免疫治療的療效。
(2)與OXA + ASP相比,NP/OXA-ASP2具有更優的性能,其可導致腫瘤部位的乳酸水平降低25.4%,細胞毒性T淋巴細胞的比例提高1.53倍,調節性T細胞的比例降低2.20倍,抑瘤率提高1.39倍。綜上所述,該研究開發的NP/OXA-ASP2是一種集腫瘤代謝調節和免疫調節等多功能于一體的新平臺,其有望進一步推動臨床化學-免疫療法的發展。
Jiazhen Yang. et al. Glucose Metabolism-Targeted Poly(amino acid) Nanoformulation of Oxaliplatin(IV)-Aspirin Prodrug for Enhanced Chemo-Immunotherapy. Advanced Materials. 2025
DOI: 10.1002/adma.202419033
https://advanced.onlinelibrary.wiley.com/doi/10.1002/adma.202419033



















