環二核苷酸(CDNs)是干擾素基因刺激因子(STING)的天然激動劑,可引發針對腫瘤的有效免疫反應。然而,低穩定性、快速清除、細胞攝取不足和低效的細胞質基質定位等問題仍會嚴重阻礙親水、帶負電的2',3'-環-GMP-AMP(cGAMP)的治療效果。如何有效地將cGAMP遞送到內質網(ER)以激活STING和進行免疫啟動成為了一項亟待攻克的難題。有鑒于此,首都醫科大學附屬北京兒童醫院梅冬教授和北京大學陳斌龍研究員構建了一種對pH響應的富胍STING納米激動劑(nPGSA),并將其用于實現cGAMP的細胞質基質遞送。
本文要點:
(1)與游離的cGAMP相比,nPGSA可實現增強的細胞內化(高達37.4倍)。pH敏感性和胍功能化的設計策略有助于快速釋放和內核體逃逸,從而能夠實現cGAMP的精準ER靶向和STING敏化的33.9倍擴增。
(2)實驗結果表明,nPGSA可調節腫瘤相關巨噬細胞(TAM)極化,進而能夠在黑色素瘤和神經母細胞瘤小鼠模型中引發有效的抗原特異性細胞免疫反應,以實現持續的腫瘤消退。綜上所述,該研究設計了一種有效的cGAMP遞送策略,為探究cGAMP通過調節腫瘤免疫微環境實現癌癥免疫治療的功能提供了新的見解。
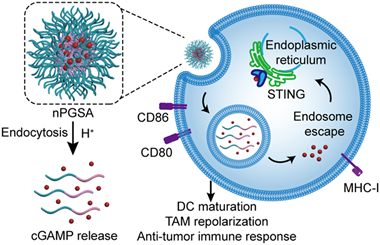
Xiao Lu. et al. A pH-Responsive and Guanidinium-Rich Nanoadjuvant Efficiently Delivers STING Agonist for Cancer Immunotherapy. ACS Nano. 2025
DOI: 10.1021/acsnano.4c10202
https://pubs.acs.org/doi/10.1021/acsnano.4c10202



















