骨關節炎(OA)是一種普遍的退行性疾病,并且缺乏有效的治療策略。氧化應激是導致OA的主要因素之一。然而,針對氧化應激的治療方法目前仍然非常有限。有鑒于此,溫州醫科大學張小磊研究員和周一飛教授在體外建立了氧化應激誘導的軟骨細胞死亡模型,并篩選了有望能夠抑制氧化應激誘導的細胞死亡的藥物。
本文要點:
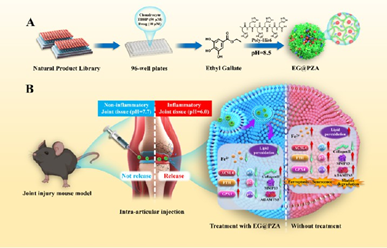
(1)在天然產物庫的600多種藥物中,沒食子酸乙酯(EG)是最有效的抗氧化應激誘導細胞死亡的藥物。然而,缺乏合適的給藥系統仍會導致生物利用度低、作用時間短和療效差等問題。因此,研究者設計了聚-His6-鋅組裝體(PZA),并構建了一種負載EG的pH響應性金屬有機框架(MOF)(EG@PZA),以用于OA治療。研究發現,EG@PZA具有溶酶體逃逸特性,可大大提高EG的利用率。
(2)EG@PZA可在酸性微環境中表現出增強的EG釋放能力。體內外研究結果表明,EG@PZA能夠在軟骨細胞中有效抑制氧化應激誘導的細胞外基質降解、鐵死亡和衰老,并在內側半月板失穩(DMM)小鼠的體內模型中有效改善OA。綜上所述,該研究開發的EG@PZA是一種具有藥物控釋作用的納米材料,可實現有效的OA治療。
Yu Chen. et al. High-Throughput Screening Strategy and Metal?Organic Framework-Based Multifunctional Controlled-Release Nanomaterial for Osteoarthritis Therapy. ACS Nano. 2025
DOI: 10.1021/acsnano.4c15740
https://pubs.acs.org/doi/10.1021/acsnano.4c15740



















