小干擾RNA(siRNA)的內(nèi)溶酶體降解會顯著降低由非病毒系統(tǒng)遞送的RNA干擾(RNAi)的有效性。利用高爾基體/內(nèi)質(zhì)網(wǎng)(Golgi/ER)運輸可以幫助siRNA繞過內(nèi)溶酶體降解途徑,但該方法往往也會導致siRNA釋放不足,并增加Golgi/ER介導的胞吐作用的風險。有鑒于此,四川大學何勤教授和李曼教授利用由細胞穿透性聚二硫化物和硫酸軟骨素組成的納米復合物開發(fā)了兩種不同的策略,以增強靶向內(nèi)化、高爾基體轉(zhuǎn)運和負載siRNA的快速細胞質(zhì)釋放。
本文要點:
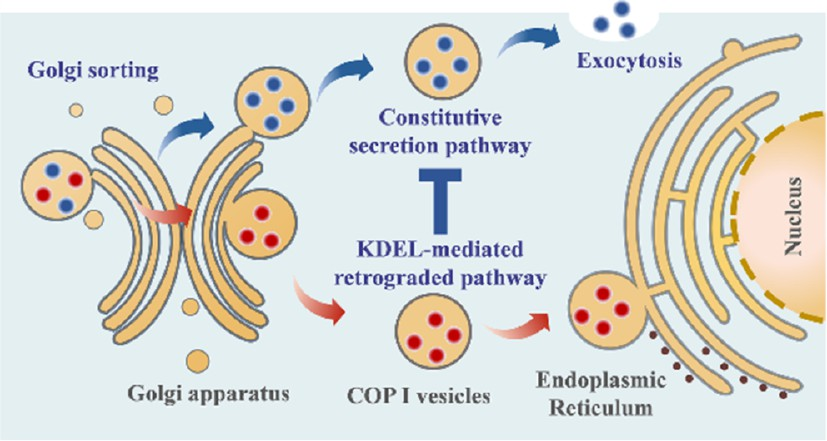
(1)在第一種策略中,莫能菌素可通過抑制胞吐作用和自噬降解等機制協(xié)同增強RNAi。在第二種策略中,實驗引入了一種基于KDEL肽介導的逆行轉(zhuǎn)運的“定向分選”方法。KDEL肽與硫酸軟骨素的結(jié)合可促進高爾基體到內(nèi)質(zhì)網(wǎng)的轉(zhuǎn)運,以減少“隨機”Golgi/ER相關(guān)的胞吐作用。研究發(fā)現(xiàn),這兩種策略的交替操作可實現(xiàn)具有顯著治療作用的高效RNAi。
(2)實驗結(jié)果表明,在使用抗Bcl-2 siRNA的小鼠黑色素瘤模型中,這些策略可分別實現(xiàn)87.1和90.1%的腫瘤抑制率。綜上所述,該研究設(shè)計的基于“靶向”和“錨定”Golgi/ER的策略能夠為克服siRNA高效遞送面臨的細胞內(nèi)化、胞內(nèi)釋放和胞吐作用等挑戰(zhàn)提供一個有效的解決方案。
Yashi Wang. et al. Dual Strategies Based on Golgi Apparatus/Endoplasmic Reticulum Targeting and Anchoring for High-Efficiency siRNA Delivery and Tumor RNAi Therapy. ACS Nano. 2025
DOI: 10.1021/acsnano.4c14778
https://pubs.acs.org/doi/10.1021/acsnano.4c14778
![]()



















