盡管已有研究開發了多種用于抗腫瘤治療的控制釋放系統,但脫靶副作用仍然是一個亟待解決的難題。通過生物相容性物質原位合成治療藥物是一種更安全、更精準的方法。有鑒于此,澳門大學王瑞兵教授和深圳大學高成教授開發了一種乏氧啟動的超分子自由基系統,其能夠誘導細胞內聚合,以破壞4T1細胞內的細胞骨架和細胞器。
本文要點:
(1)該系統利用可被腫瘤的乏氧和還原性環境選擇性還原的2:1超分子主-客體復合物(由葫蘆[7]脲(CB[7])和苝酰二亞胺衍生物(PDI)組成,PDI+2CB[7])產生離域自由基陰離子。研究發現,CB[7]能夠有效地穩定這些陰離子,進而可在4T1細胞內使PDI+2CB[7]復合物與2-羥乙基甲基丙烯酸酯(HEMA)發生自由基聚合。
(2)實驗結果表明,該原位聚合能夠顯著破壞腫瘤代謝,產生強烈的抗腫瘤反應,并且不會造成嚴重的全身毒性。綜上所述,該研究證明了由穩定的內源性刺激誘導的超分子自由基可以引發胞內聚合反應,從而能夠為實現無需常規化療藥物的選擇性、有效的抗腫瘤治療提供一個新的策略。
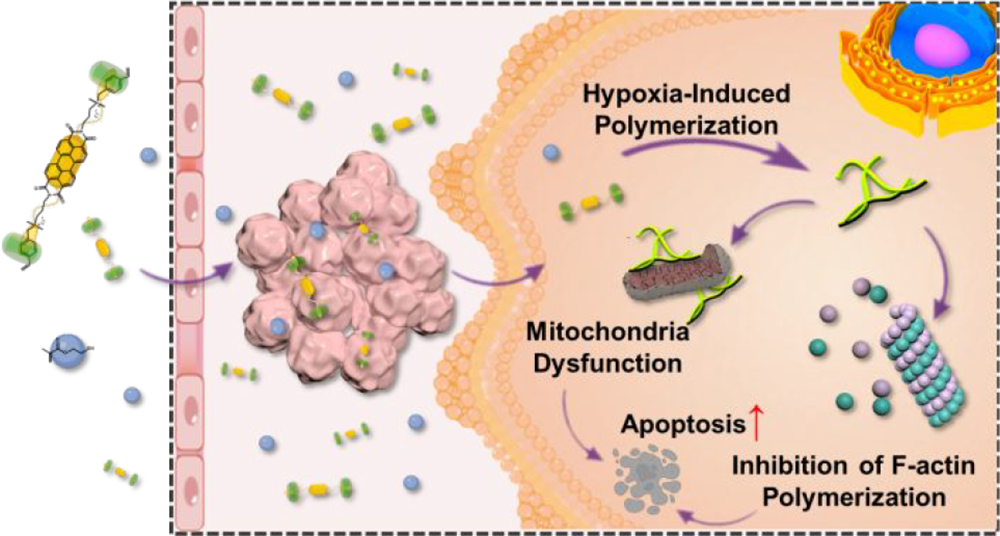
Mian Tang. et al. Hypoxia-Initiated Supramolecular Free Radicals Induce Intracellular Polymerization for Precision Tumor Therapy. Journal of the American Chemical Society. 2025
DOI: 10.1021/jacs.4c14847
https://pubs.acs.org/doi/10.1021/jacs.4c14847



















