雖然傳統(tǒng)觀念認(rèn)為蛋白冠是一種障礙物,但其也可以促進(jìn)靶向藥物遞送系統(tǒng)的發(fā)展。有鑒于此,吉林大學(xué)陳芳芳教授、Yuansong Bai和劉海巖教授設(shè)計(jì)了一種利用帶有凝集蛋白(NAPs)的納米顆粒靶向急性髓系白血病(AML)的新方法。
本文要點(diǎn):
(1)NAPs中的凝集轉(zhuǎn)鐵蛋白和C3b能夠與髓系白血病細(xì)胞過(guò)表達(dá)的CD71和CD11b受體發(fā)生選擇性結(jié)合。體外研究發(fā)現(xiàn),NAPs可在白血病細(xì)胞中實(shí)現(xiàn)高達(dá)73.9%的多柔比星(DOX)攝取率(游離藥物為6.19%),并且能夠?qū)⒄<?xì)胞中的脫靶積累從42.9%顯著降低到5.76%。
(2)實(shí)驗(yàn)結(jié)果表明,NAPs的體內(nèi)分布與白血病細(xì)胞的器官浸潤(rùn)模式相關(guān)。在體外和體內(nèi)NSG小鼠模型中,NAPs能夠通過(guò)凋亡和鐵死亡等機(jī)制誘導(dǎo)細(xì)胞死亡,進(jìn)而表現(xiàn)出抗白血病活性。綜上所述,該研究開(kāi)發(fā)的NAP介導(dǎo)的靶向給藥方法是一種極具發(fā)展前景的AML治療策略,其可以提高治療效果,并最大限度地減少脫靶效應(yīng)。
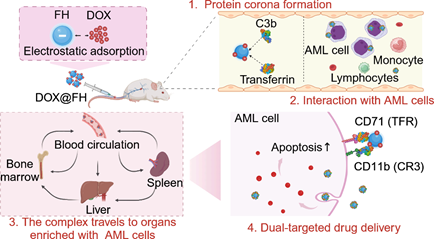
Wen Wu. et al. Dual-Targeted Drug Delivery to Myeloid Leukemia Cells via Complement- and Transferrin-Based Protein Corona. Nano Letters. 2024
DOI: 10.1021/acs.nanolett.4c04429
https://pubs.acs.org/doi/10.1021/acs.nanolett.4c04429



















