放射治療可利用高能射線精準靶向和根除腫瘤細胞,其在多種惡性腫瘤的治療領域中具有關鍵作用。然而,腫瘤固有的低放射敏感性和免疫抑制微環境等問題仍會嚴重阻礙放療的有效性。有鑒于此,北京大學深圳醫院穆婧研究員、新加坡國立大學陳小元院士和Qing You設計了一種將過氧亞硝酸鹽(ONOO-)介導的放射增敏與腫瘤相關中性粒細胞(TANs)極化相結合的新策略,并將其用于逆轉免疫抑制腫瘤微環境(TME)和增強放射治療的效力。
本文要點:
(1)實驗將X射線激活的鑭系摻雜閃爍體(LNS)與光敏NO前驅體進行串聯,實現了ONOO-的原位生成。研究發現,LNS-RS納米平臺可通過響應腫瘤部位過表達的GSH釋放共負載的TGF-β抑制劑SB525334,以促進TANs從N2表型重編程為N1表型,從而能夠有效地將促瘤微環境轉變為抑瘤狀態。
(2)實驗結果表明,該“組合拳”療法可觸發產生強大的抗腫瘤免疫反應,其能夠在原位結直腸癌和黑色素瘤小鼠模型中表現出強有力的治療效果,并有效地預防轉移性結直腸癌的肝轉移和復發。綜上所述,該研究構建的X射線活化平臺能夠激活多種治療方式,有望為實現基于放療的腫瘤協同治療開辟一條新的途徑。
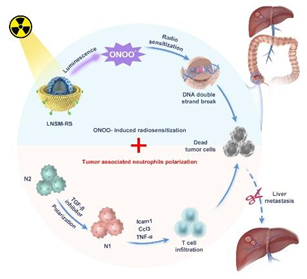
Hui Li. et al. X-ray-Activated Nanoscintillators Integrated with Tumor Associated Neutrophils Polarization for Improved Radiotherapy in Metastatic Colorectal Cancer. Biomaterials. 2024
https://www.sciencedirect.com/science/article/pii/S0142961224005672



















