盡管增強的滲透性和滯留性(EPR)效應能夠用于實體腫瘤的被動靶向治療,但EPR效應的異質性仍會導致多種納米藥物難以產生有效的臨床結果。因此,了解EPR效應的機制對于克服納米藥物的臨床轉化面臨的挑戰至關重要。有鑒于此,東南大學張宇教授、涂景教授和武昊安研究員建立了一種可靠的方法,即利用聯合的放射基因組學和臨床磁共振成像(MRI)技術以及基因集通路富集分析揭示影響納米顆粒(NP)通過EPR效應轉運到腫瘤中的關鍵因素。
本文要點:
(1)實驗構建了聚乳酸-羥基乙酸(PLGA)包覆的Fe3O4 NPs造影劑,并通過MRI觀察和定量分析了NPs的單層和多層分布,從而提高了MRI評價血管通透性的準確性。
(2)通過基因本體(GO)和京都基因和基因組數據庫(KEGG)對基因和通路的富集分析,研究者發現了多種影響血管通透性的基因,如Cldn1、Dlg2、Bves、Prkag3、Cldn10和Cldn8,它們與腫瘤血管的緊密連接有關,并且能夠控制腫瘤血管的通透性。綜上所述,該研究設計了一種MRI支持、能夠增加從遺傳篩選中收集的數據廣度的方法,有望為臨床患者的分層和個性化治療奠定重要的理論基礎。
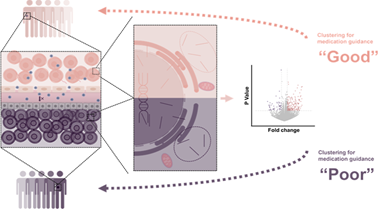
Di Liu. et al. Magnetic Resonance Imaging-Based Radiogenomic Analysis Reveals Genomic Determinants for Nanoparticle Delivery into Tumors. ACS Nano. 2024
DOI: 10.1021/acsnano.4c09387
https://pubs.acs.org/doi/10.1021/acsnano.4c09387



















