編輯總結(jié)
碳-氮鍵是現(xiàn)代藥物的基石,化學(xué)家們不斷努力尋找更高效的方法來構(gòu)建它們。兩項最新研究分別報道了將碳-碳雙鍵斷裂并在其位置形成碳-氮三鍵的不同方法。Br?gger 等人使用高價碘試劑合成了腈類化合物,而 Cheng 等人則采用了異相銅催化劑與氧氣協(xié)同作用的方法。在這兩種情況下,碳-碳雙鍵都充當(dāng)了便捷的反應(yīng)位點,使得多種復(fù)雜分子的轉(zhuǎn)化成為可能。——Jake S. Yeston
研究背景
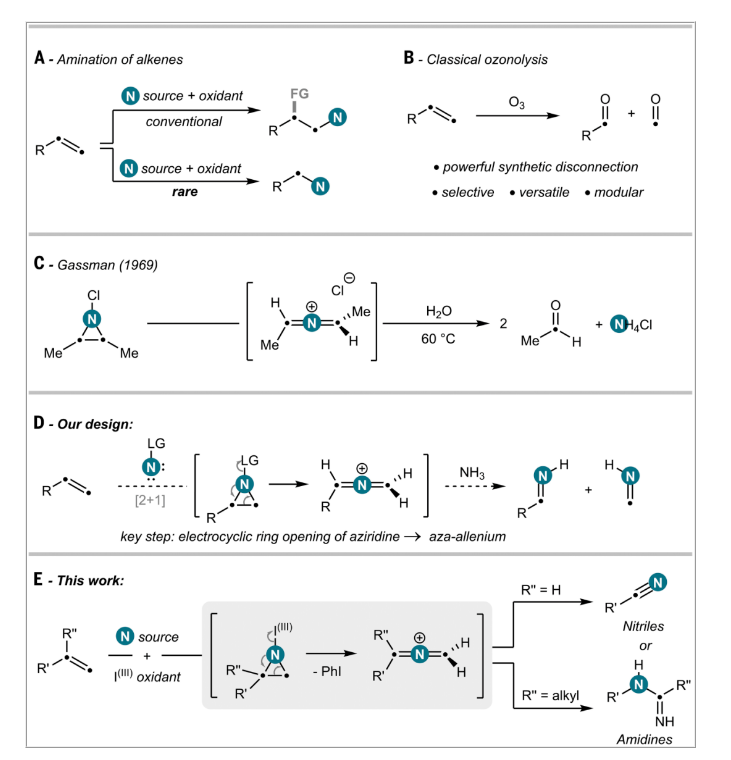
碳氮鍵的生成反應(yīng)是現(xiàn)代有機合成中的一個重要的領(lǐng)域。研究通過碳-氮(C–N)鍵的形成合成含氮分子,對于藥物、農(nóng)用化學(xué)品和材料的研發(fā)及制備至關(guān)重要。針對這一問題,蘇黎世聯(lián)邦理工學(xué)院Bill Morandi教授團隊在Science期刊上發(fā)表了題為“Oxidative amination by nitrogen atom insertion into carbon-carbon double bonds”的最新論文。他們報道了一種直接向非活化碳-碳雙鍵插入氮原子的方法,以獲得氮丙二烯(aza-allenium)中間體。該中間體可根據(jù)初始烯烴的取代模式進一步轉(zhuǎn)化為腈或脒類化合物。這一操作簡便且具有高度官能團兼容性的反應(yīng)適用于多種非活化烯烴。 市售廉價的高價碘試劑 PIFA 是該反應(yīng)的關(guān)鍵。作者的機理假設(shè)得到了化學(xué)捕獲實驗的支持,同時該實驗也證明了該方法在合成重要的含氮雜環(huán)化合物方面的實用性。此外,該方法還可作為合成酰胺、胺以及 1?N 標(biāo)記分子的通用策略。
研究亮點
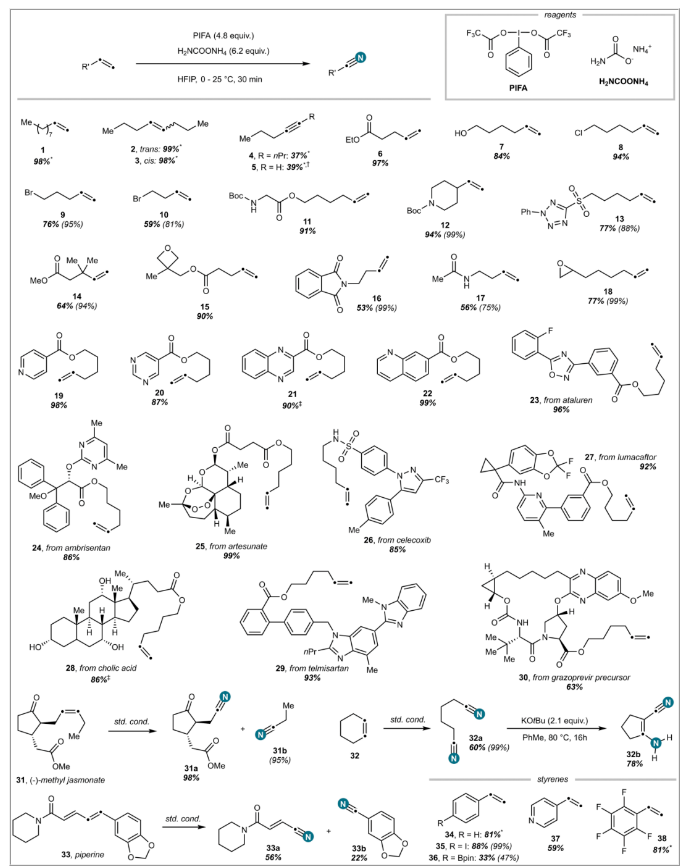
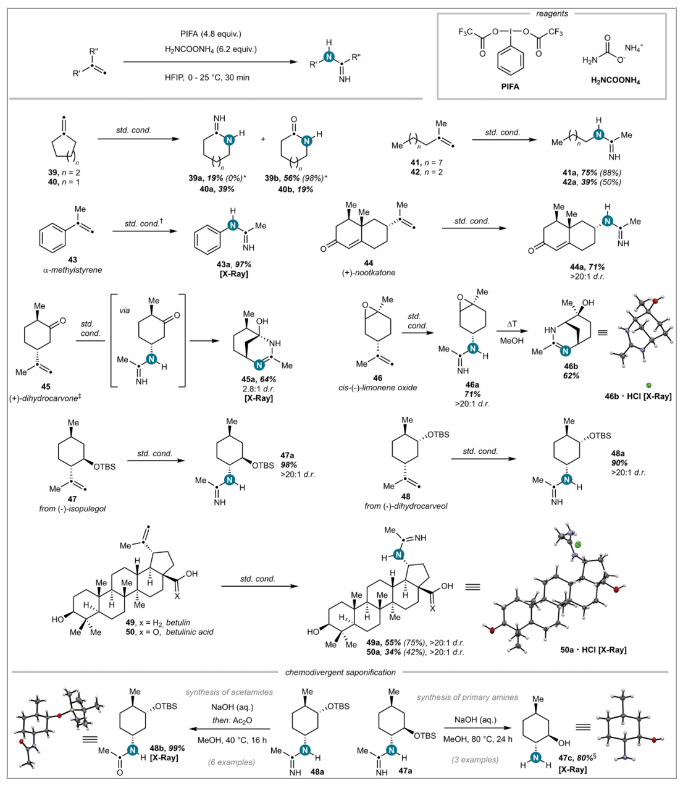
(1)實驗首次開發(fā)了一種通過氮雜環(huán)丙烷生成氮丙二烯中間體,并利用氧化反應(yīng)實現(xiàn)烯烴直接氧化胺化的方法,成功獲得了多種腈類化合物。該方法具有廣泛的官能團兼容性,能夠在多種端基和內(nèi)烯烴的基礎(chǔ)上高效進行反應(yīng),且反應(yīng)條件簡便。(2)實驗通過原位形成 N–LG 氮雜環(huán)丙烷,經(jīng)過開環(huán)反應(yīng)形成瞬時氮丙二烯中間體,并用氨等親核試劑截獲該中間體,成功實現(xiàn)了烯烴的直接氧化胺化。該過程不僅簡化了傳統(tǒng)的多步合成路線,還展示了優(yōu)異的收率和區(qū)域選擇性。(3)實驗發(fā)現(xiàn),1,1-二取代烯烴在該反應(yīng)條件下經(jīng)歷了獨特的氮雜-Beckmann 重排,產(chǎn)生了脒類產(chǎn)物,并保持了優(yōu)異的立體選擇性。這為反應(yīng)提供了新的合成途徑,擴展了該方法的應(yīng)用范圍。
圖文解讀
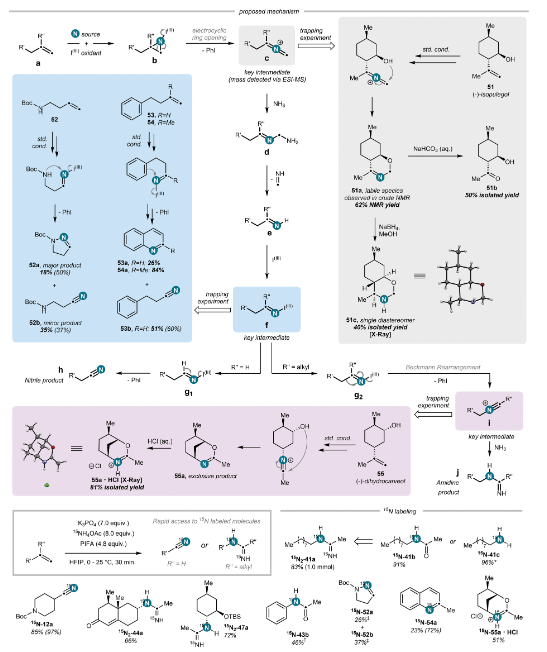
圖4. 未活化烯烴氧化胺化的機理研究和15N標(biāo)記研究
結(jié)論展望
本研究開發(fā)了一種氧化胺化反應(yīng),其中線性烯烴被裂解為腈類,分支烯烴轉(zhuǎn)化為脒類。作者提出了一種機制,涉及氮原子插入非活化烯烴的C(sp2)–C(sp2)鍵,利用瞬態(tài)的氮丙二烯中間體進行合成應(yīng)用。該反應(yīng)操作簡便,無需排除空氣或水分,且與多種官能團兼容。從更廣泛的角度來看,這項研究表明,氮原子插入烯烴能夠形成氮丙二烯物種,作為具有廣泛合成應(yīng)用潛力的反應(yīng)性氮含中間體,為下游的多樣化反應(yīng)提供了優(yōu)異的潛力,并為發(fā)現(xiàn)和制備重要的氮含化合物開辟了新的途徑。 Yannick Br?gger et al. ,Oxidative amination by nitrogen atom insertion into carbon-carbon double bonds.Science387,1108-1114(2025).DOI:10.1126/science.adq4980